Тест с ответами по теме Общие свойства металлов
1 Металлическая связь – это связь между …
A) молекулами металлов
B) атомами и ионами металлов
C) положительными ионами металлов, атомами металлов и свободными электронами в кристаллической решетке
D) положительными ионами металлов и протонами
2. До изобретения электронной фотовспышки для освещения объекта в закрытом помещении использовали возгорание
A) Фосфора
B) Натрия
C) Магния
D) Серы
E) Рубидия
E) ионами металлов
3 Железный гвоздь не вытесняет металл из раствора его соли:
A) Хлорида олова (II)
B) Хлорида меди (II)
C) Хлорида никеля (II)
D) Хлорида натрия
E) Хлорида свинца (II)
4 В стакан с 490 г 10%-ной серной кислоты опустили цинковую пластину. Через некоторое время масса пластины изменилась на 13 г. Объем (в литрах, н.у.) выделившегося газа
A) 1,24 л B) 2,24 л C) 22,4 л D) 4,48 л
E) 5,56 л
5 Для металлов характерен тип химической связи:
A) Металлическая
B) Ионная
C) Ковалентная неполярная
D) Водородная
E) Ковалентная полярная
6 Бронза – сплав меди с:
A) Серебром и добавками P, Si, Zn, Au
B) Цинком и добавками Ni, Ag, Si
C) Оловом и добавками Al, Mn, Be, Si, Ni, Fe
D) Магнием, марганцем и добавками Sn, Al, K, Hg
E) Никелем и добавками Pb, Mn, Pt
7 В схеме Ca → Ca(OH)2 → CaO → CaF2 → HF требуется провести электролиз расплава на этапе
A) F2 HF
B) CaF2 F2
C) Ca Ca(OH)2
D) Ca(OH)2 CaO
E) CaO CaF2
8Имеется хлорид элемента III группы, в котором элемент проявляет высшую валентность и содержит 79,68% хлора. Относительная атомная масса элемента и химический знак
A) 11 В
B) 70 Ga
C) 45 Sc
D) 27 Al
E) 56 Fe
9. Массовые доли железа и кислорода в минерале Fe3O4
A) 72,4% и 27,6%
B) 36,2% и 66,8%
C) 40,4% и 53,6%
D) 70% и 30%
E) 64,6% и 35,4%
10 Металл, который был известен 5000-4500 лет до н.э.
A) Серебро
B) Рутений
C) Уран
D) Цезий
E) Скандий
11 Масса меди (г), которая образуется при взаимодействии 0,1 моль железа с 75 г 20%-ного сульфата меди (II)
A) 6,0
B) 8,9
C) 25,6
D) 24,0
E) 6,8
12 Наибольшую молярную массу имеет оксид
A) BaO
B) SrO
C) CaO
D) BeO
E) MgO
13. Группа металлов, которые можно получить алюминотермическим способом:
A) Ni, Cr, Zn
B) K, Na, Cr
C) Cu, Na, Cr
D) Cs, Cu, Fe
E) Na, Mn, Al
14 В ряду оксидов Na2O → MgO → Al2O3 → SiO2 → P2O5 происходит
A) Возрастание, затем уменьшение кислотных свойств
B) Возрастание основных свойств
C) Уменьшение амфотерных свойств
D) Возрастание кислотных свойств
E) Уменьшение кислотных свойств
15. В электротехнике для производства ламп накаливания используют металлическую нить из:
A) Fe
B) Zn
C) W
D) Cu
E) Al
16 К основаниям относятся:
A) Cu(OH)2, HCl
B) Ba(OH)2, CO2
C) NaNO3, H3PO4
D) NaOH, Ca(OH)2
E) KNO3, Ba(OH)2
17 На 4 г оксида магния подействовали избытком галогеноводорода. Образовалось 9,5 г соли. Формула галогеноводорода
A) HF
B) HBr
C) HAt
D) HI
E) HCl
18. Взаимодействуют 5 моль сульфида натрия и 5 моль хлорида меди (II). Характер среды раствора, после проведения реакции
A) слабокислый
B) слабо-щелочной
C) нейтральный
D) щелочной
E) кислый
19 Электролизом раствора нельзя получить металл
A) Sn
B) Pb
C) Cu
D) Ca
E) Fe
20 Лантаноиды расположены в периоде номер
A) 7
B) 3
C) 6
D) 5
E) 4
21. В самородном состоянии встречается металл:
A) Ag
B) K
C) Al
D) Ca
E) Pb
22. Из приведенных оксидов – SiO2, SnO2, Na2O, Al2O3, CrO3, MnO – к амфотерным относятся
A) MnO и SiO2
B) SnO2 и Al2O3
C) Na2O и Al2O3
D) MnO и Al2O3
E) Al2O3 и CrO3
23 Только электролизом расплава можно получить группу металлов
A) Cs, Al, Cu
B) Na, Cu, Ag
C) K, Ca, Mg
D) Fe, Ca, Hg
E) Li, Ag, Sn
24 Металлическая связь в веществе
A) KCl
B) S
C) HCl
D) P
E) Ba
25 При растворении в соляной кислоте 10,4 г смеси железа и магния выделилось 6,72 л водорода (н.у.). Масса железа в смеси
A) 5 г
B) 5,6 г
C) 6,7 г
D) 3 г
E) 4,4 г
26 Хлорид алюминия реагирует с
A) Серебром.
B) Медью.
C) Железом.
D) Цинком.
E) Кальцием.
27 В алюмотермических процессах алюминий играет роль
A) ингибитора
B) восстановителя
C) катализатора
D) окислителя
E) удаляет шлаки из руд
28. При обработке 9 г смеси алюминия и меди хлороводородной кислотой выделилось 5,6 л (н.у.) газа. Массовая доля (в %) меди в смеси
A) 60%
B) 30%
C) 40%
D) 20%
E) 50%
29. Скорость реакции взаимодействия металлов с соляной кислотой уменьшается в ряду
A) Fe, Mg, Zn, Na, Cu
B) Na, Mg, Zn, Fe, Cu
C) Mg, Cu, Zn, Na, Fe
D) Cu, Na, Mg, Zn, Fe
E) Zn, Fe, Mg, Cu, Na
30 Не является сплавом цветных металлов
A) Никелин
B) Электрон
C) Латунь
D) Бронза
E) Серый чугун
31 Наименьшая масса соли будет затрачена при получении 1 моль HCl действием серной кислоты на хлорид
A) Магния
B) Лития
C) Алюминия
D) Натрия
E) Калия
32 Сплав алюминия с кремнием называется:
A) Силумином
B) Бронзой
C) Латунью
D) Сталью
E) Мельхиором
33 При взаимодействии железа с раствором, содержащим 32 г сульфата меди (II) в раствор перейдет число частиц железа
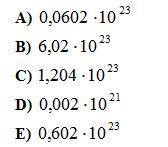
34Схема алюмотермического процесса:
A) Al + NaOH →
B) Al + C →
C) Al2O3 + HCl →
D) MnO2 + Al →
E) Al2O3 + H2SO4 →
35 В природе чаще всего калий и хром находятся в виде (соответственно):
A) Солей
B) Свободном
C) Оксидов и оснований
D) Солей и оксидов
E) Оснований
Конец теста по теме Общие свойства металлов
1C 3C 3D 4D 5A 6C 7B8D 9A10A11A 12A 13A 14D 15C 16D 17B18C 19D 20C 21A 22B 23C24E 25D26E 27B28E 29B 30E31B 32A33C 34D35A

Ваше имя:
Ваш email: