Тест с ответами по теме Металлы побочных подгрупп
1. В состав гемоглобина входит ион металла:
A) Fe (II)
B) Zn
C) Cu (II)
D) Mg
E) Fe (III)
2Железо будет выделять водород из:
A) Гидроксида натрия (конц.)
B) Раствора серной кислоты
C) Гидроксида аммония
D) Концентрированной азотной кислоты
E) Концентрированной серной кислоты
3. Масса оксидов свинца (II) и олова (IV), необходимая для получения 500 г припоя, состоящего из 34% олова и 66% свинца
A) 175 г SnO2 и 342 г PbO
B) 216 г SnO2 и 356 г PbO
C) 216 г SnO и 399 г PbO
D) 205 г SnO2 и 396 г PbO
E) 183 г SnO и 351 г PbO
4 Электронная конфигурация иона Fe2+
A) 1s2 2s2 2p6 3s2 3p6 3d0
B) 1s2 2s2 2p6 3s2 3p6 3d5 4s1
C) 1s2 2s2 2p6 3s2 3p6 3d6
D) 1s2 2s2 2p6 3s2 3p6 3d5
E) 1s2 2s2 2p6 3s2 3p6 3d5 4s2
5 Железо нельзя получить:
A) Восстановлением лимонита углем
B) Восстановлением магнетита водородом
C) Электролизом водных растворов солей железа (II)
D) Нейтрализацией гидроксидов железа
E) Восстановлением гематита водородом
6. Из приведенных оксидов – CrO, Al2O3, CO, P2O5 – с водным раствором гидроксида натрия взаимодействуют:
A) CrO и CO
B) Al2O3 и P2O5
C) Al2O3 и CO
D) CO и P2O5
E) CrO и P2O5
7 Превращение Fe → FeO → Fe2O3 → Fe соответствует переходу
A) … 3d5 4s1 … 3d6 4s2 … 3d5 3d6
B) … 3d6 4s2 … 3d6 … 3d6 4s2 3d5
C) … 3d6 4s2 … 3d6 … 3d5 3d6 4s2
D) … 3d6 … 3d6 4s1 … 3d6 3d5 4s2
E) … 3d6 4s2 … 3d5 … 3d6 4s2 3d5
8 Продукты FeSO4 и Н2О соответствуют взаимодействию реагентов:
A) Fe и H2SO4 (10%)
B) Fe и H2SO4 (96%)
С) FeO и H2SO4
D) Fe2 O 3 и H2SO4
E) FeO и H2SO3
9 При восстановлении водородом смеси оксидов железа (II) и железа (III) массой 37 г получено железо массой 28 г. Массовая доля (в %) каждого из оксидов в смеси
A) 73% FeO и 27% Fe2 O 3
B) 68% FeO и 32% Fe2 O3
C) 65% FeO и 35% Fe 2O3
D) 90% FeO и 10% Fe 2O3
E) 83% FeO и 17% Fe2O3
10. Реактивами на ионы Fe2+ и Fe3+ являются соответственно
A) K3[Fe(CN)6] и K4[Fe(CN)6]
B) K4[Fe(CN)6] и KCl
C) KCl и K3[Fe(CN)6]
D) K4[Fe(CN)6] и KCNS
E) K3[Fe(CN)6] и NaCl
11Веществом А в схеме превращений
Cr → Cr2O3 ---+NaCl---> X ---+NaOH---> Y --+NaCl(p-p)---> A может быть
A) Na2CrO2
B) Na2CrO4
C) Cr(OH)2
D) Na[Cr(OH)4]
E) Cr(OH)3
12 В схеме превращений
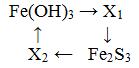
Веществами Х1 и Х2 могут быть
A) Х1 – FeO, X2 – Fe2(SO4)3
B) X1 – FeO, X2 – FeBr3
C) X1 – FeCl3, X2 – Fe(NO3)3
D) X1 – FeO, X2 – FeSO4
E) X1 – Fe2O3, X2 – FeCl2
13 Для полного осаждения серебра из 170 г 1%-ного раствора AgNO3 потребовалось 100 мл иодоводородной кислоты. Молярность раствора HI равна
A) 1М
B) 0,01М
C) 10М
D) 0,1М
E) 1,1М
14 При растворении в соляной кислоте 10,4 г смеси железа и магния выделилось 6,72 л водорода (н.у.). Масса железа в смеси
A) 6,7 г
B) 5 г
C) 4,4 г
D) 5,6 г
E) 3 г
15 В схеме превращений
Fe ---Cl2---> A ---NaOH---> Б ---(температура 0 градусов по цельсию)---> В ---HCl---> Г
вещества А, В, Г
A) FeCl3, Fe2O3, FeCl3
B) FeCl2, Fe, FeCl3
C) FeCl2, FeO, FeCl2
D) FeCl3, FeO, FeCl2
E) FeCl3, Fe2O3, FeCl2
16 В схеме превращений
Fe + HNO3 Fe(NO3)3 + NO + H2O
сумма коэффициентов в сокращенном ионном уравнении равна
A) 9
B) 8
C) 10
D) 12
E) 11
17 В стакан с 490 г 10%-ной серной кислоты опустили цинковую пластину. Через некоторое время масса пластины изменилась на 13 г. Объем (в литрах, н.у.) выделившегося газа
A) 1,24 л B) 2,24 л C) 22,4 л D) 4,48 л
E) 5,56 л
18 Красный цвет крови из-за
A) аминогруппы в гемоглобине
B) азотистых оснований в гемоглобине
C) углеводов в гемоглобине
D) гемов, которые содержат III валентное железо в оксигемоглобине
E) остатков фосфорной кислоты в гемоглобине
Ответы к тесту по теме Металлы побочных подгрупп
1A 2B 4C 5D6B7C 8B9A10A11D12C 13D14D 15A16A17B18D
-
X
Ваше имя:
Ваш email:

Татьна 21 December 2021 08:41