Итоговый тест(10 класс-ЕМ)
Итоговый тест(10 класс-ЕМ)
1 вариант
1.Какое количество фосфора содержится в образце массой 15,5 г: А) 1 моль, В) 0,5 моль, С) 2 моль, D) 0,25 моль, Е) 3 моль?
2.Определите реакцию соединения: А) Ni2++2OH-→Ni(OH)2 В) 2Na+CL2→2NaCL С) Fe0+Cu2+→ Fe2++Cu0 D) Cu(OH)2→CuO+H2O, Е) 2НС!+Са→СаС!2+Н2
3.Число неспаренных электронов в атоме азота: А) 1 В)2 С) 3 D) 5, Е) 4..
4. В какой молекуле только ковалентная полярная связь: А) С12, В) Н2 С) НС1
D) КС1 Е) C2H5ONa?
5.В каком случае реакция между ионами не протекает: А) Ag++CL-
В) Ca 2++CO3 2- С) 3K++ PO4 3-D) Ba2++SO4 2- Е) 2Са2++2С1-?
6. Сумма всех коэффициентов в уравнении реакции
Na2CO3 + HCl NaCl + H2O + CO2
A) 3 B) 5 C) 7 D) 9 E) 1
7. Расставьте коэффициенты на основании электронного баланса и укажите , чему равен коэффициент окислителя в уравнении: CuS+HNO3→Cu(NO3)2+H2SO4+NO2+H2O: А) 5 В) 8 С) 10 D) 12 Е) 9
8. . Какой элемент проявляет более сильные окислительные свойства:
A) Pb B) Ag C) S D) O E) Na?
9. Сколько моль MgSO4 образуется при реакции 6г Мg и Н2SO4?
А) 0,125 моль, В) 0,25 моль, С) 0,37моль, D) 0,5 моль,Е) 0,4 моль?.
10. Определите степень окисления серы в серной кислоте: А) +2, В)+4, С)+6
D) -2. Е) +3
11. В каком случае взята разбавленная серная кислота?
A) Zn+H2SO4→H2S+..
B) Pb+H2SO4→SO2+..
C) Zn+ H2SO4→ H2+..
D) Ag+H2 SO4→SO2+..
E) Mg+ H2SO4→H2S+?
12. В электротехнике для производства ламп накаливания используют металлическую нить из:
A) Fe
B) Zn
C) W
D) Cu
E) Al
13. Раствор хлорида алюминия имеет среду:
A) Индифферентную
B) Кислую
C) Нейтральную
D) Слабощелочную
E) Щелочную
14 Продукты FeSO4 и Н2О соответствуют взаимодействию реагентов:
A) Fe и H2SO4 (10%)
B) Fe и H2SO4 (96%)
С) FeO и H2SO4
D) Fe2 O 3 и H2SO4
E) FeO и H2SO3
15.Из 142 кг СаО получили 182 кг гашёной извести. Каков выход продукта реакции в(%) от теоретически возможного: A) 80,B) 98, C) 100,D) 25 E) 50%
16 Нашатырный спирт-это
А) твёрдый хлорид аммония,
В) раствор хлорида аммония в воле
С) раствор аммиака в воде,
Д) раствор сульфата аммония
Е) раствор нитрата аммония
17. Фосфор – только восстановитель в химической реакции:A) 2P + 3Ba = Ba3P2
В)2P + 3H2 = 2H3P
С)2P + 3Cl2 = 2PCl3
Д) P + 3K = K3P
Е) 4Р+5О2=2Р2О5
18. Формула кислой соли
A) K2NaPO4
B) MgSO4
C) Mg(OH)Cl
D) KHSO4
E) Na[Al(OH)4]
19. Сместит равновесие влево в процессе
СО (г) + 2Н2 (г) ↔СН3ОН (г) + Q
A) повышение давления
В)понижение концентрации СН3ОН
С) повышение концентрации Н2
Д) повышение температуры
Е)понижение температуры
20. Сумма коэффициентов в полном ионном уравнении КОН+Н2SO4 равна А) 10
В) 11, С) 13 Д)14, Е) 15
21. Масса нитрата серебра, необходимого для осаждения хлорида серебра из 104 г 20%-ного раствора хлорида бария, составляет А) 32 г, В) 33 г, С) 34 г, Д) 30 г, Е) 31 г.
22. Формулы неизвестных веществ в схеме:Zn ---> ZnO ---> ZnCl2 --+NaOH--> ?
A) Zn(OH)2; ZnCl2
B) NaCl; Zn(OH)2
C) Zn(OH)2; ZnO
D) Zn; Zn(OH)2
E) Zn(OH)2; Na2[Zn(OH)4]
23 Для сжигания кремния количеством вещества 0,5 моль потребуется кислород объемом (н.у.)
A) 11,2 л
В) 1,12 л
С) 5 л
Д) 0,5 л
Е) 1,5л
24 Даны: а) MgCl2 б) J2 в) HClO г) NaClO4 д) KClO3
Ряд веществ с окислительно-восстановительной двойственностью
A) в, г, д
B) а, в, г
C) б, в, д
D) а, б, д
E) б, в, г
25.Реакция протекает до конца между ионами
A) Al3+ и SO42-
B) Mg3+ и NO3-
C) Ca2+ и CO32-
D) Na+ и Cl-
E) Ba2+ и ОН-
2 Вариант
1.Какое количество вещества содержится в оксиде углерода IV массой 4,4 г: А) 1моль,В) 0,5 моль, С)О,2 моль, Д) 0, 1 моль, Е) 3 моль?
2. К какому типу относится реакция HNO3+KOH→KNO3+H2O: А) замещения б) соединения С) обмена,
Д) разложения, Е) обратимая?
3. Вид связи в оксидах углерода (II) и (IV):
A) Ковалентный неполярный
В) Ионный
С) Металлический
Д) Ковалентный полярный
Е) водородный
4. Элемент 2 периода со степенью окисления -4,+2, +4- это:
А)сера, В)азот,С) углерод,Д) кремний, Е) магний.
5. Группа амфотерных оксидов
A) Al2O3, MnO2, CO2
B) MnO2, SO2, Al2O3
C) Al2O3, ZnO, BeO
D) K2O, CuO, BeO
E) ZnO, SO3, MnO2
6. В каком случае реакция пойдёт до конца?
А) MgSO4+Ba(NO3)2→
В) BaCL2+Mg(NO3)2→
С) MgCL2+Ba(NO3)2→
Д) BaSO4+Mg(NO3)2→
7. Массовая доля алюминия в оксиде алюминия:
A) 59% B) 35% C) 38% D) 53% E) 49%
8. Даны вещества: FeCL3 NaNO3 H3PO4 Na2S CaBr2 Сколько веществ реагирует с AgNO3 А) 1 В) 2 С) 3 Д) 4 , Е) 5?
9. Не подвергается гидролизу соль: А) нитрат цинка, В) бромид аммония, С) силикат калия, Д) хлорид калия, Е) карбонат натрия
10.Сумма индексов в формулах аллотропных модификаций кислорода
А) 3,В) 4 С) 6 Д) 5 Е) 2
11 Валентность и степень окисления азота в азотной кислоте равны
A) V и +5 B) V и -5 C) IV и +5 D) IV и +3 E) V и +3
12. У какого атома окислительные свойства выражены сильнее:
А) …3s23p5
В) .. 2s22p5
С) .. 5s25p5
Д) … 3d10 4s24p5
Е) …….2s22p4?
13. Сумма всех коэффициентов в полном ионном уравнении взаимодействия силиката калия и фосфорной кислоты равна: А) 24 В) 27 С) 28, Д) 26 Е) 25
14 Степень окисления азота в ряду NH3 NO N2
A) Сначала повышается, а потом понижается
B) Повышается
C) Сначала понижается, а потом повышается
D) Понижается
E) Не изменяетсякая
15. Масса негашёной извести получится при прокаливании 2 кг известняка, если массовая доля примесей в нём 5%: A) 1,06 кг B) 1,5кг
C) 1,9 кг, D) 2,3 кг E) 1,4 кг?
16 Железный гвоздь не вытесняет металл из раствора его соли:
A) Хлорида олова (II)
B) Хлорида меди (II)
C) Хлорида никеля (II)
D) Хлорида натрия
E) Хлорида свинца (II)
17. Повышение температуры сместит химическое равновесие в сторону прямой реакции:
A) 2SO2 + O2 ↔ 2SO3 + Q
B) SO2 + H2O ↔ H2SO3 + Q
C) CO + H2O ↔ CO2 + H2 + Q
D) N2O4 ↔ 2NO2 - Q
E) CO2 + H2O ↔ H2CO3 +
18.Количество электронов в катионе Fe+3
A) 29 B) 26 C) 23 D) 22 E) 25
19. Объём аммиака, полученного при взаимодействии 12л азота и 30л водорода при 20%-ном выходе продукта реакции, составляет: А) 3л, В) 1л, С) 5л, Д) 4л.Е) 2л
20. Сумма коэффициентов в левой части уравнения реакции
H2S + KMnO4 = K2SO4 + MnO2 + KOH + H2O
А) 9 В)5 С)11 Д)7 Е)8
21 К керамическим изделиям не относится:
A) Фарфоровая тарелка
B) Керамические трубы
C) Хрустальная ваза
D) Кирпич
E) Облицовочная плитка
22.Формулы соединений (a, b, d) и условие протекания реакции (с) по схеме:
С СО2 СаСО3 СаО СаС2
A) а – H2O; b – CaC2; c – давление p; d – CH4
B) a – O2; b – H2CO3; c – to; d – CO
C) a – O2; b – Ca(OH)2; c – to; d - C
D) a – O2; b – K2CO3; c – to; d – CO2
E) a – CO; b – Ca; c – to; d – CO
23. При взаимодействии 3 моль оксида алюминия и 294 г серной кислоты, получится количество вещества соли (в молях)
A) 2
B) 3
C) 5
D) 4
E) 1
24. Масса окислителя, взаимодействующего с 2 моль восстановителя по схеме НС1+О2→Н2О+С12 составляет: А) 8 г В) 32 г С) 71 г Д) 16г Е) 64г
25 Кислотный оксид образует
A) Ba
B) Cu
C) Si
D) Ca
E) Na
Вариант 3
1.Число частиц Al(NO3)3 в 21,3 г
A) 0,12 молекул B) 1,48 молекул
C) 6 молекул D) 1,68 молекул
E) 0,6 молекул
2. Атом состоит из:
A) протонов и нейтронов
B) ядра и вращающихся вокруг него нейтронов
C) протонов и электронов
D) ядра и вращающихся вокруг него электронов
E) нейтронов и электронов
3. Изменение давления не влияет на реакцию, находящуюся в состоянии равновесия:
А)2CO + O2 2CO2
В)2SO2 + O2 2SO3
С)NH3 N2 + 3H2
Д) N2 + O2 2NO
Е) 2Н2+О2 2Н2О
4.Какие реакции относятся к окислительно-восстановительным:
1) Zn+ Cu CL2 -> ZnCL2 + Cu
2) ZnCL2 + 2NaOH -> Zn (OH)2 +2NaCL
3) Zn (OH)2 +2NaOH -> NaZnO2 +2H2O
4) 2Zn + O2 -> 2ZnO
5) Zn (OH)2 -> ZnO+H2O
6) 2Zn(NO3)2 -> 2ZnO +4NO2+O2
А) 1, 5, 6 В) 1,4,6, С) 1,3,5, Д) 1,3,4, Е)1,2,3.
5.Молекула какого вещества в пространстве имеет форму равностороннего треугольника: А) NH3, В) BCL3 С) PH3 Д) N2 Е) NCL3?
6.Какой объём воздуха потребуется для окисления глюкозы массой 45 г? А) 16л, В) 160л,С) 80 л, Д) 320л, Е) 40л.
7..Какие из попарно взятых веществ будут в растворе вступать в реакцию: A) KCl+Na2SO4 B) Li OH+H2SO4 C) Mg CL2+KNO3 D) NаOH+H2SO4 E) Cu CL2+HCL?
8.Сколько граммов 80%-ного технического карбида кальция потребуется для получения 2,8 л ацетилена (н.у.)? А) 14 г, В) 16 г, С) 10 г, Д) 78 г, Е) 12 г.
9.Сколько теплоты выделится при сжигании 2,4 г магния по термохимическому уравнению: 2Mg+O2→2Mg O+1127 кдж.? А) 1127 кдж, В) 102 кдж, С) 56,35 кдж, Д) 112,70 кдж, Е) 28,175 кдж.
10.Какая связь в соединении элементов с зарядами ядер +14 и +8? А) ионная, В) ковалентная полярная, С) ковалентная неполярная, д) металлическая, Е) водородная.
11.Число электронов, которое может принять атом азота равно: А) 5,В) 2, С) 3, Д) 1 Е) 4
12.У какого из следующих атомов металлические свойства выражены сильнее: А)…3s23p2 В)… 4s2 С)… 3s23p6 Д)… 3d104s2 Е).. 5s1 ?
13.При разложении 18 г воды выделится объём кислорода (выход 20%): А) 10л, В) 8,96, С) 11,2л, Д) 8л, Е) 12л
14..Объем водорода (при н.у.), который образуется при взаимодействии 0,6 моль уксусной кислоты с 0,5 моль металлического натрия, равен:
A) 11,2 л б) 44,8 л в) 5,6 л г) 22,4 л
д) 89,6 л
15Необратимая химическая реакция проходит при сливании растворов: А) ZnSO4+HCL,
В) MgCL2+HNO3 С) ZnSO4+KOH Д) KOH+NaCL .Е) СаС12+КОН
16. Ряд солей, подвергающихся гидролизу
A) MgSO4, K2SO4 B) Na2SO4, Ba(NO3)2
C) FeCl2, CrSO4 D) BaCl2, MgSO4
E) FeCl3, NaNO3
17.Число электронных слоёв в атоме элемента,содержащего в ядре 20 протонов: А) 3 В) 6 С) 4 Д) 5 Е)2.
18.Какой элетролит образует при диссоциации только ОН-ионы? А) Н2О В) СН3СООН С) NaOH Д) Zn(OH)2, Е) А!(ОН)3?
19 Какая из схем выражает реакцию замещения?
А) Н2+О2→ В) Н2+СиО→ С) СиС12+КОН→
Д) СиО+НС1→. Е) КОН+НС1→
20. В схеме превращений
Fe + HNO3 Fe(NO3)3 + NO + H2O
сумма коэффициентов в сокращенном ионном уравнении равнаA) 9 B) 8 C) 10 D) 12 E) 11
21. В схеме превращений
Fe A Б В Г вещества А, В, Г
A) FeCl3, Fe2O3, FeCl3
B) FeCl2, Fe, FeCl3
C) FeCl2, FeO, FeCl2
D) FeCl3, FeO, FeCl2
E) FeCl3, Fe2O3, FeCl2
22. Схеме превращений
S2- → S0 → S+4 → S+6 → S-2
Может соответствовать превращение
A) H2S → S → SO2 → H2 →SO3
B) Na2S → S → SO3 → SO2 → S
C) FeS → SO2 → SO3 →S → H2S
D) FeS2 → S →SO3 → SO2 → H2S
E) H2S → S → SO2 → SO3 → H2S
23. Какой из металлов взаимодействует с разбавленной серной кислотой: А) Ag В) Cu С) Hg Д) Fe. Е) Аи?
24. В какой реакции образуется гидроксид кальция?
А) Ca+HCL→ В) CaO+H2O→
С) CaO+H3PO4→ Д) CaO+HCL→
Е) Са+Н2→ ?
25 При взаимодействии кислот с основаниями и с основными оксидами образуется
А) соль и вода, В) основной оксид
С) металл и вода Д) оксид и вода
Е) основание и вода
Вариант 4
1.Какое количество серы содержится в образце массой .6,4 г: А) 1 моль, В) 0,5 моль, С) 2 моль, D) 0,2 моль, Е) 3 моль?
2.Реакция идет до конца с выделением газа при взаимодействии: A) NaCI + H2SO4 → B) KOH + AI2(SO4)3 → C) Li2CO3 + HCI → D) BaCI2 + Mg(NO3)2 → E)Ca(OH)2 + HNO3→
3.В какой из этих реакций металл проявляет восстановительные свойства? A) Na2SO4 + BaCI2 →BaSO4 + 2NaCI B) Cu + 2H2SO4 (k) →CuSO4 +2H2O +SO2 C) K2CO3 +2HNO3→2KNO3 + H2O + CO2 D) MgO + CO2 →MgCO3 E) NaOH + HCI →NaCI + H2O
4.Коэффициент перед формулой восстановителя в уравнении реакции взаимодействия цинка с водой, равен: A) 1 B) 2 C) 3D) 4 E) 5
5 Амфотерный оксид образует
A) Bе
B) Cu
C) Si
D) Ca
E) Na
6.Валентность и степень окисления серы в серной кислоте равны
A) V и +5 B) V и -5 C) VI и +6 D) IV и +3 E) V и +3
7.Сумма всех коэффициентов в полном ионном уравнении взаимодействия силиката кальция и серной кислоты равна: А) 4 В) 7 С) 8, Д) 6 Е) 12
8.Какой элетролит образует при диссоциации только Н+ионы? А) Н2О В) СН3СООН С) NaOH Д) Zn(OH)2, Е) А!(ОН)3?
9. У какого атома востановительные свойства выражены сильнее:
А) …3s2 В) .. 2s22p5 С) .. 5s2 Д) … 3d10 4s2
Е) …….2s22p1?
9.Какой объём воздуха потребуется для окисления бензола массой 7,8 г? А) 16л, В) 160л,С) 80 л, Д) 320л, Е) 40л.
10.Изменение давления не влияет на реакцию, находящуюся в состоянии равновесия:
А) NH3 N2 + 3H2 В) N2 + O2 2NO
С) 2CO + O2 2CO2 Д) 2SO2 + O2 2SO3
11. Нашатырный спирт-это
А) твёрдый хлорид аммония,
В) раствор хлорида аммония в воле
С) раствор аммиака в воде,
Д) раствор сульфата аммония
Е) раствор нитрата аммония
12.В какой молекуле только ковалентная полярная связь: А) С12, В) Н2 С) КС1
D) НС1 Е) C2H5ONa?
13.Формулы соединений (a, b, d) и условие протекания реакции (с) по схеме:
С СО2 СаСО3 СаО СаС2
A) а – H2O; b – CaC2; c – давление p; d – CH4
B) a – O2; b – H2CO3; c – to; d – CO
C) a – CO; b – Ca; c – to; d – CO
D) a – O2; b – K2CO3; c – to; d – CO2
E) a – O2; b – Ca(OH)2; c – to; d - C
14.Какая из схем выражает реакцию замещения?
А) Н2+О2→ В) КОН+НС1→ С) СиС12+КОН→
Д) СиО+НС1→.Е) Н2+СиО→
15.При взаимодействии О,3 моль оксида алюминия и 29,4 г серной кислоты, получится количество вещества соли (в молях)
A) 12 B) 3 C) 5 D) 4 E) 9,3
16. Какой из металлов взаимодействует с разбавленной серной кислотой: А) Ag В) Cu С) Hg Д). Аи Е) Fe?
17.Число электронных слоёв в атоме элемента,содержащего в ядре 25 протонов: А) 3 В) 6 С) 4 Д) 5 Е)2.
18.Степень окисления азота в ряду РH3 Р 2O 5 Р
A) Сначала повышается, а потом понижается
B) Повышается
C) Сначала понижается, а потом повышается
D) Понижается E) Не изменяетсякая
19. Даны: а) MgCl2 б) J2 в) HClO г) NaClO4 д) KClO3
Ряд веществ с окислительно-восстановительной двойственностью A) в, г, д B) а, в, г
C) б, в, д D) а, б, д E) б, в, г
20.Формула средней солиA) K2NaPO4
B) MgSO4 C) Mg(OH)Cl
D) KHSO4 E) Na[Al(OH)4
21. Какое количество вещества содержится в оксиде серы IV массой 6,4 г: А) 1моль,В) 0,5 моль, С)О,2 моль, Д) 0, 1 моль, Е) 3 моль?
22.Не подвергается гидролизу соль: А) нитрат цинка, В) бромид аммония, С) силикат калия, Д) хлорид калия, Е) карбонат натрия
23.Продукты FeSO4 и Н2О соответствуют взаимодействию реагентов:
A) Fe и H2SO4 (10%)
B) Fe и H2SO4 (96%)
С) FeO и H2SO4
D) Fe2 O 3 и H2SO4
E) FeO и H2SO3
24.Количество электронов в катионе Fe+2
A) 29 B) 26 C) 23 D) 22 E) 24
25.В каком случае реакция между ионами не протекает: А) Ag++CL-
В) Ca 2++CO3 2- С) 3K++ PO4 3-D) Ba2++SO4 2- Е) 2Са2++2С1-?
Конец теста по теме Химия, 10 класс.
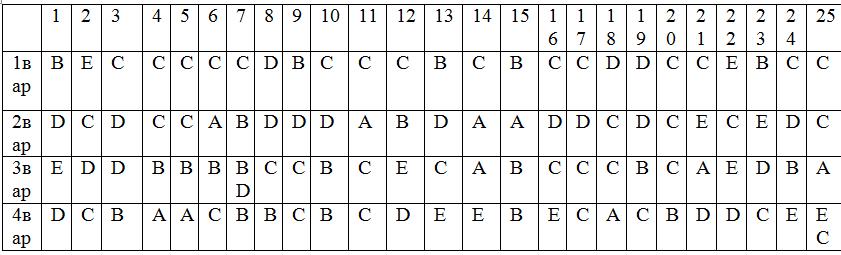
Ответы к тесту:

Ваше имя:
Ваш email: